韩国
当前韩国疫情蔓延趋势严重,询问韩国KFDA注册的较多,重点介绍一下韩国注册的相关要求:
韩国医疗器械准入的法规门槛,基本分类为I、II、III、IV类,持证为韩国公司(License holder),且韩代职责较重,如:快速通关、快速到门的服务、仓库管理,包括韩国保址部所有监管事宜而且在海关业务的应急时间等全链条内容,接受KGMP定期评审等。
KFDA的等级标准
等级I:非接触人体的或无潜在危险性的产品;
等级II:对人体具有一定的危险性但对人体生命的危险及造成的影响和危险性比较低的产品;
等级III:一定时间内插入人体使用或潜在的危险性比较高的产品;
等级IV:永久的移植到人体内或直接接触到心脏、中枢神经神经等而使用的产品;
相关流程
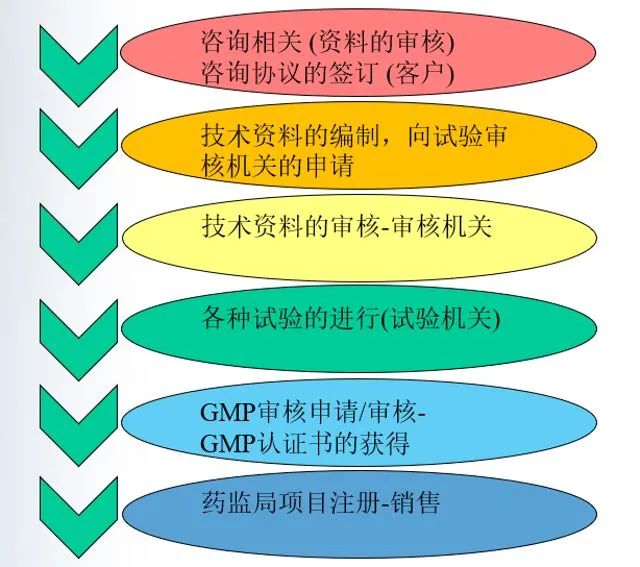
韩国注册相关内容
申请KGMP证书和接受现场审核;
对于II类产品一般是委托授权的第三方审核员完成审核(但笔者前期服务的案例中,也都是韩国保址部官员),若为III IV类产品则由韩国保址部(相当于中国药监局)自行审核,并获得KGMP证书;
寄送样品到韩国MFDS授权的实验室进行韩标的测试;
由韩代向MFDS提交技术文件(包括TCF、检测报告、KGMP证书等),同时还需要向韩国保址部缴纳申请费,后续由该机构进行注册文件的审核,最终获得批准,后续方可入市。额温枪属于韩国II类产品,预计周期示样品而定。
联系我们
讯科检测是国家认可委CNAS、中国计量认证CMA、ISTA国际安全运输协会等国际机构的认可实验室。XKS的使命:让您的产品通全球!
业务咨询:0755-23312011


